
吃瑞舒伐他汀和依折麦布,几周后复查血脂,血脂控制已达标,医生让停用瑞舒伐他汀,可以吗?
极目新闻通信员任艺萱
近日,最新一期海外化学限制的顶级期刊《AngewandteChemieInternationalEdition》(德国应用化学,SCI一区TOP,影响因子IF:17)在线发表武汉大学东谈主民病院(湖北省东谈主民病院)泌尿外科团队与武汉大学药学院互助的最新询查扫尾。该询查在海外上初次系统地将PROTAC介导的卵白降解与纳米酶涵养的铁圆寂相汇注,为攻克去势相背性前哨腺癌(CRPC)耐药性提供了新的念念路,并为纳米PROTAC的临床更始奠定了基础。
该扫尾题为“Nanozyme-MediatedPROTACsDeliveryforTargetedProteinDegradationandFerroptosisSensitizationinProstateCancer”(纳米酶介导的PROTAC寄递用于前哨腺癌中的靶向卵白降解与铁圆寂增敏)。武汉大学东谈主民病院泌尿外科程帆西宾、刘凌琪副西宾,武汉大学药学院黎威西宾为共同通信作家,武汉大学博士询查生王陈媛、江雪、雷嘉鹏为共同第一作家。询查获取国度当然科学基金和湖北省当然科学基金的撑抓。
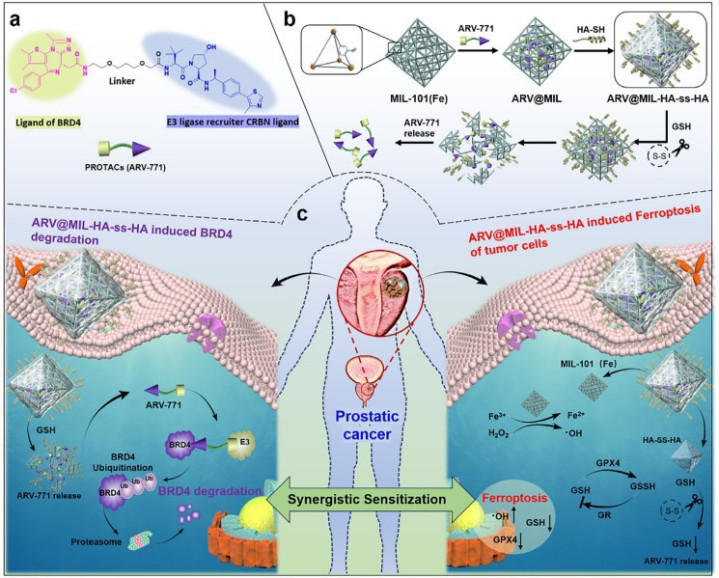
去势相背性前哨腺癌(CRPC)是现时前哨腺癌治愈中的主要临床挑战,尽管AR拮抗剂在一定过程上改善了患者预后,但耐药性险些不行幸免。连年来,卵白靶向降解嵌合体(PROTAC)药物如ARV-771,通过涵养BRD4卵白降解,可灵验扼制AR/AR-v7的转录活性,展现出纯粹的治愈后劲。关连词,该类药物存在水溶性差、体内巩固性低、靶向性不及等问题,限制了其临床更始。与此同期,铁基MOF材料MIL-101不仅可当作药物载体,还具备类过氧化物酶(POD)和过氧化氢酶(CAT)活性,福州股票配资大致通过催化肿瘤微环境中的H₂O₂生成羟基摆脱基(·OH)并消费谷胱甘肽(GSH),从而涵养肿瘤细胞铁圆寂。因此,若能将ARV-771与MIL-101汇注,并赋予其主动靶向与反映性开释能力,有望终了PROTAC介导的靶向卵白降解与铁圆寂的协同增效,为CRPC治愈提供新战术。
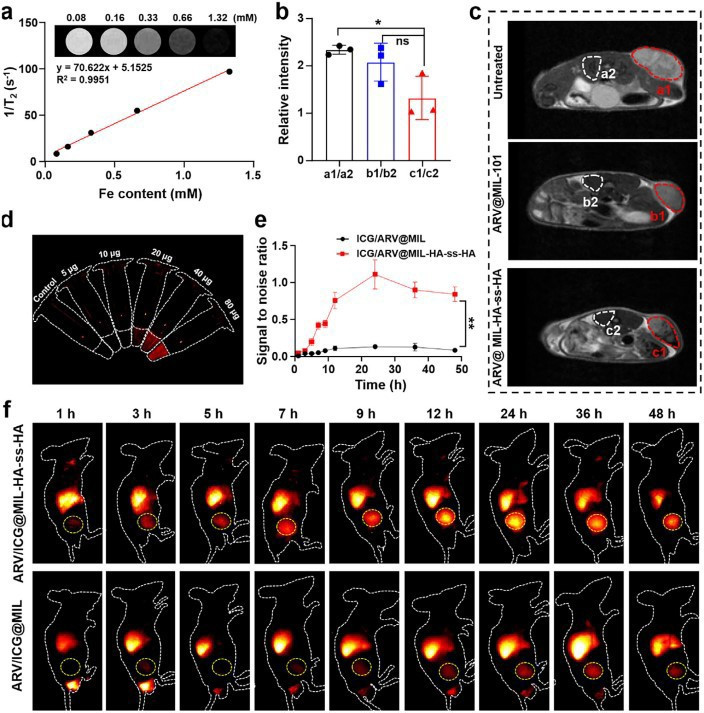
本询查谋略并构建了一种多功能纳米PROTAC平台ARV@MIL-HA-ss-HA,其中枢念念路是行使铁基MOFMIL-101当作载体负载ARV-771,并在名义修饰由二硫键交联的透明质酸(HA-ss-HA)水凝胶。该水凝胶一方面通过HA与肿瘤细胞高抒发的CD44受体互相作用终了主动靶向,另一方面在肿瘤细胞内高GSH环境中发生二硫键断裂,触发药物反映性开释。MIL-101载体自己可当作纳米酶,在肿瘤细胞内催化H₂O₂生成·OH并消费GSH,涵养铁圆寂;同期开释的ARV-771通过降解BRD4卵白,既成功扼制肿瘤滋长,又进一步增强细胞对铁圆寂的敏锐性,从而终了双重协同治愈。询查通过体外细胞践诺、卵白组学分析、体内肿瘤模子、MRI与荧光成像等时代,系统评估了该纳米平台的靶向性、药物开释特色、BRD4降解能力、铁圆寂涵养效应、抗肿瘤疗效及生物安全性。
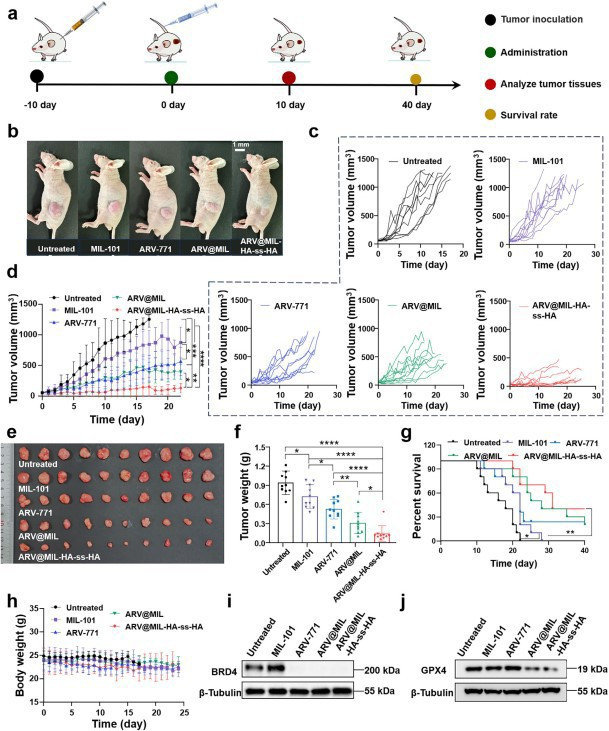
本询查证据该新式纳米PROTAC平台ARV@MIL-HA-ss-HA,可通过将铁基MOFMIL-101的纳米酶活性与PROTAC药物ARV-771的靶向卵白降解功能相汇注巨牛盈app,终了对CRPC的高效协同治愈。体外与体内践诺均证据,该战术显赫进步了药物的肿瘤富集、BRD4降解效力、铁圆寂涵养能力及抗肿瘤疗效,同期展现出纯粹的生物安全性。本项询查初次系统地将PROTAC介导的卵白降解与纳米酶涵养的铁圆寂相汇注,为克服CRPC耐药性提供了新的念念路,并为纳米PROTAC的临床更始奠定了基础。
联丰优配官网盛达优配红藤网配资垒富优配正中优配宏泰配资提示:文章来自网络,不代表本站观点。